- Оглавление
- Молекулярная физика. Термодинамика Основные законы и формулы
- Молекулярная физика Основные формулы
- Основы термодинамики
- Тема 1. Законы сохранения в механике
- Колебания
- Трансформатор
- Волны
- Кинематика
- Равномерное движение по окружности
- Импульс
- Электрический ток
- Энергобаланс замкнутой цепи
- Электролиз
- Статика
- Магнетизм
- Гидростатика
- Электростатика
- Расширенная PDF версия документа “Все главные формулы по школьной физике”
- Оптика
- Атомная и ядерная физика
- Ядерные реакции
Оглавление
Релятивистское сокращение длины:
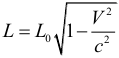
Релятивистское удлинение времени события:

Релятивистский закон сложения скоростей. Если два тела движутся навстречу друг другу, то их скорость сближения:
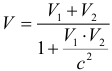
Релятивистский закон сложения скоростей. Если же тела движутся в одном направлении, то их относительная скорость:

Энергия покоя тела:

Любое изменение энергии тела означает изменение массы тела и наоборот:

Полная энергия тела:
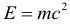
Полная энергия тела Е пропорциональна релятивистской массе и зависит от скорости движущегося тела, в этом смысле важны следующие соотношения:

Релятивистское увеличение массы:
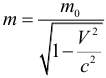
Кинетическая энергия тела, движущегося с релятивистской скоростью:

Между полной энергией тела, энергией покоя и импульсом существует зависимость:

Молекулярная физика. Термодинамика Основные законы и формулы
Уравнение
состояния идеального газа (уравнение
Клапейрона–Менделеева)pV
= RT
Масса молекулыm0
= M/NA
Количество
вещества ν
= m/ M, ν = N / NA
Средняя кинетическая
энергия молекулы
Внутренняя
энергия идеального газа
Средняя
квадратичная скорость молекулы
Средняя
арифметическая скорость молекулы
Количество
теплоты, необходимое для нагревания
телаQ
= cm∆T
Удельная
теплоёмкость газа при постоянном
объёме
Удельная
теплоёмкость газа при постоянном
давлении
Среднее
число соударений молекулы
в единицу
времени
Средняя
длина свободного пробега молекулы
Закон диффузии
(закон Фика)
Закон
теплопроводности (закон Фурье)
Работа
газа при изобарном расширении
Работа
газа при изотермическом расширении
Работа
газа при адиабатном расширении
Уравнения
адиабатного процесса (уравнения
Пуассона)
Термический
КПД тепловой машиныη
= (Q1–Q2)
/ Q1
Термический
КПД идеальной тепловой машины (цикла
Карно)η
= (T1–T2)
/ T1
Высота
подъёма жидкости в капиллярной трубке
Молекулярная физика Основные формулы

m — масса;
μ — молярная масса вещества;
N — число молекул;
NA = 6,02·1023 моль-1 — число Авогадро
2 Основное уравнение молекулярно-кинетической теории идеального газа

p — давление идеального газа;
m — масса одной молекулы;
n = N/V — концентрация молекул;
V — объем газа;

— среднее значение квадрата скорости молекул.
3 Средняя квадратичная скорость молекул идеального газа

k = 1,38·10-23 Дж/К — постоянная Больцмана;
R = kNA = 8,31 Дж/(моль·К) — универсальная газовая постоянная;
T = t+273 — абсолютная температура;
t — температура по шкале Цельсия.
4 Средняя кинетическая энергия молекулы одноатомного газа

5 Давление идеального газа

n — концентрация молекул;
k — постоянная Больцмана;
T — абсолютная температура.
6 Закон Бойля-Мариотта

p — давление;
V — объем газа.
7 Закон Шарля
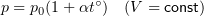
p0 — давление газа при 0 °С;
α = 1/273 °C-1 — температурный коэффициент давления.
8 Закон Гей-Люссака

V0 — объем газа при 0 °С.
9 Уравнение Менделеева-Клапейрона

10 Объединенный закон газового состояния (уравнение Клапейрона)

11 Закон Дальтона

pi — парциальное давление i-й компоненты смеси газов.
Основы термодинамики

ν — количество вещества;
R = 8,31 Дж/(моль·К) — универсальная газовая постоянная;
2 Элементарная работа, совершаемая газом,
при изменении объема на бесконечно малую величину dV

p — давление газа.
При изменении объема от V1 до V2

3 Первый закон термодинамики

ΔQ — количество подведенной теплоты;
ΔA — работа, совершаемая веществом;
ΔU — изменение внутренней энергии вещества.
4 Теплоемкость идеального газа

ΔQ — количество переданной системе теплоты на участке процесса;
ΔT — изменение температуры на этом участке процесса.
1.
Основное уравнение молекулярно-кинетической
теории газов
Р = nkT,
n = N/V,
где N– число молекул, содержащихся в данной
системе;V– объем.
3. Средняя
кинетическая энергия поступательного
движения молекулы
4. Средняя
кинетическая энергия молекулы
где i– число
степеней свободы молекулы.
5. Средняя
квадратичная скорость молекулы
где k– постоянная
Больцмана;Т– абсолютная температура;m0– масса молекулы;μ– молярная масса;R– универсальная
газовая постоянная.
6. Средняя
арифметическая скорость молекулы
7.
Наиболее вероятная скорость молекулы
= m/ μ = N/NA,
где m– масса
вещества;μ– его молярная масса;N– число молекул;NA– число
Авогадро.
9.
Уравнение состояния идеального газа
(уравнение Менделеева –Клапейрона)
где Р– давление
газа в сосуде;V– объем сосуда;m– масса газа, содержащегося в данном
сосуде;μ– молярная масса газа;R– универсальная газовая постоянная;Т– абсолютная температура.
10.
Изотермический процесс (Т = const,m
= const)
11.
Изохорический процесс (V = const,m =
const)
P = P0
(1+
t)
или
P1/P2
= T1/T2,
где t– температура
по шкале Цельсия;T– температура
по шкале Кельвина;–
температурный коэффициент.
12.
Изобарический процесс (Р =const,m =const)
V = V0(1+
t)
или V1/V2= T1/T2.
13. Работа
расширения газа:
A = P V;
A= – ν СVΔТ,
где V– изменение объема;R– универсальная
газовая постоянная; ν– количество
вещества; СV – теплоемкость
при постоянном объеме;Т– изменение температуры.
14.
Внутренняя энергия идеального газа
U=(ν
RT)(i/2)
= ν СVТ,
15.
Удельные теплоемкости газа:
16.
Уравнение Майера для удельных теплоемкостей
ср – сv = R/μ.
где γ = Ср /
Сv =(i
+ 2)/i, Ср,Сv– молярные теплоемкости при постоянном
давлении, объеме.
18. Связь между
удельной (с) и молярной (С)
теплоемкостями
c = С/μ.
19.
Уравнение теплового баланса
где Q– количество
теплоты, необходимое для нагревания
тела массойmот температурыt1до температурыt2;c– удельная теплоемкость вещества.
Q = m,
где – удельная теплота плавления вещества.
Q = r m,
где r– удельная
теплота парообразования вещества.
22. Первый
закон термодинамики
Q = U + A,
где Q– количество
теплоты, сообщенное термодинамической
системе;U– изменение внутренней энергии системы;А– работа, совершенная системой
против внешних сил.
23.
Коэффициент полезного действия цикла
Карно
= (Q1–Q2)/Q1=(T1–T2)
/T1,
где Q1–
количество теплоты, полученное от
нагревателя;Q2– количество
теплоты, переданное холодильнику;Т1– абсолютная температура нагревателя;Т2– абсолютная температура
холодильника.
24.
Разность энтропий двух состояний ВиА
25. Закон
распределения молекул по скоростям
(закон Максвелла)
где ΔN– число
молекул, относительные скорости которых
лежат в интервале отuдо (u + Δu);u =υ/υв– относительная
скорость, гдеυ– данная скорость,υв– наиболее вероятная скорость молекул;Δu– величина интервала относительных
скоростей, малая по сравнению со скоростьюu.
где Ph–
давление газа на высотеh;P0– давление на высотеh = 0;g–
ускорение свободного падения.
27.
Средняя длина свободного пробега молекул
газа
28. Общее
число столкновений всех молекул в
единице объема за единицу времени
где V– изменение объема;R– универсальная
газовая постоянная; ν– количество
вещества;сv –
удельная теплоемкость при постоянном
объеме;Т–
изменение температуры.
Соседние файлы в папке Ким, Ляховский, Маторин-Физика
В первом полугодии 10 класса мы занимаемся механикой, МКТ и термодинамикой (Темы 1 — 5 плюс Тема Х): именно эти темы доминируют на заключительных этапах перечневых олимпиад, которые проходят в феврале-марте. Иногда там появляются также задачи по электростатике (Тема 6), которую начинаем обычно в январе.
Оставшиеся Темы 7 и 8 мы проходим весной по окончании олимпиадного сезона: это уже подготовка к олимпиадам 11 класса.
В каком объёме заниматься каждой темой — я решаю с каждым учеником индивидуально.
Ссылки на уроки (теория) ведут на лекции Павла Виктора.
Тема 1. Законы сохранения в механике
Механическая работа рассчитывается по следующей формуле:
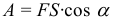
Самая общая формула для мощности (если мощность переменная, то по следующей формуле рассчитывается средняя мощность):

Мгновенная механическая мощность:

Коэффициент полезного действия (КПД) может быть рассчитан и через мощности и через работы:

Формула для кинетической энергии:

Потенциальная энергия тела поднятого на высоту:

Потенциальная энергия растянутой (или сжатой) пружины:

Полная механическая энергия:
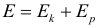
Связь полной механической энергии тела или системы тел и работы внешних сил:

Закон сохранения механической энергии (далее – ЗСЭ). Как следует из предыдущей формулы, если внешние силы не совершают работы над телом (или системой тел), то его (их) общая полная механическая энергия остается постоянной, при этом энергия может перетекать из одного вида в другой (из кинетической в потенциальную или наоборот):
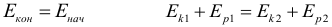
Колебания
Уравнение описывающее физические системы способные совершать гармонические колебания с циклической частотой ω0:

Решение предыдущего уравнения является уравнением движения для гармонических колебаний и имеет вид:

Период колебаний вычисляется по формуле:
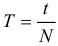

Циклическая частота колебаний:
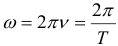
Зависимость скорости от времени при гармонических механических колебаниях выражается следующей формулой:
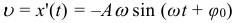
Максимальное значение скорости при гармонических механических колебаниях:
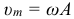
Зависимость ускорения от времени при гармонических механических колебаниях:
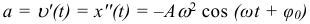
Максимальное значение ускорения при механических гармонических колебаниях:
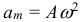
Циклическая частота колебаний математического маятника рассчитывается по формуле:

Период колебаний математического маятника:
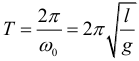
Циклическая частота колебаний пружинного маятника:
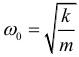
Период колебаний пружинного маятника:
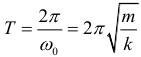
Максимальное значение кинетической энергии при механических гармонических колебаниях задаётся формулой:

Максимальное значение потенциальной энергии при механических гармонических колебаниях пружинного маятника:

Взаимосвязь энергетических характеристик механического колебательного процесса:

Энергетические характеристики и их взаимосвязь при колебаниях в электрическом контуре:
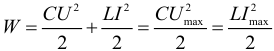
Период гармонических колебаний в электрическом колебательном контуре определяется по формуле:

Циклическая частота колебаний в электрическом колебательном контуре:
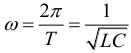
Зависимость заряда на конденсаторе от времени при колебаниях в электрическом контуре описывается законом:
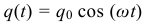
Зависимость электрического тока протекающего через катушку индуктивности от времени при колебаниях в электрическом контуре:
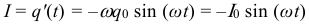
Зависимость напряжения на конденсаторе от времени при колебаниях в электрическом контуре:

Максимальное значение силы тока при гармонических колебаниях в электрическом контуре может быть рассчитано по формуле:

Максимальное значение напряжения на конденсаторе при гармонических колебаниях в электрическом контуре:

Переменный ток характеризуется действующими значениями силы тока и напряжения, которые связаны с амплитудными значениями соответствующих величин следующим образом. Действующее значение силы тока:

Действующее значение напряжения:

Мощность в цепи переменного тока:

Трансформатор
Если напряжение на входе в трансформатор равно U1, а на выходе U2, при этом число витков в первичной обмотке равно n1, а во вторичной n2, то выполняется следующее соотношение:
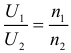
Коэффициент трансформации вычисляется по формуле:
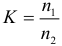
Если трансформатор идеальный, то выполняется следующее соотношение (мощности на входе и выходе равны):

В неидеальном трансформаторе вводится понятие КПД:

Волны
Длина волны может быть рассчитана по формуле:

Разность фаз колебаний двух точек волны, расстояние между которыми l:
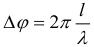
Скорость электромагнитной волны (в т.ч. света) в некоторой среде:

Скорость электромагнитной волны (в т.ч. света) в вакууме постоянна и равна с = 3∙108 м/с, она также может быть вычислена по формуле:
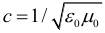
Скорости электромагнитной волны (в т.ч. света) в среде и в вакууме также связаны между собой формулой:

При этом показатель преломления некоторого вещества можно рассчитать используя формулу:

Кинематика
Путь при равномерном движении:
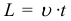
Перемещение S (расстояние по прямой между начальной и конечной точкой движения) обычно находится из геометрических соображений. Координата при равномерном прямолинейном движении изменяется по закону (аналогичные уравнения получаются для остальных координатных осей):

Средняя скорость пути:

Средняя скорость перемещения:
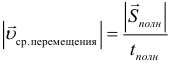
Определение ускорения при равноускоренном движении:
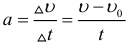
Выразив из формулы выше конечную скорость, получаем более распространённый вид предыдущей формулы, которая теперь выражает зависимость скорости от времени при равноускоренном движении:
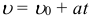
Средняя скорость при равноускоренном движении:

Перемещение при равноускоренном прямолинейном движении может быть рассчитано по нескольким формулам:

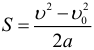
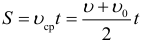
Координата при равноускоренном движении изменяется по закону:
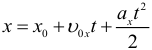
Проекция скорости при равноускоренном движении изменяется по такому закону:
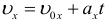
Скорость, с которой упадет тело падающее с высоты h без начальной скорости:

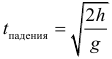
Время падения тела с высоты h без начальной скорости:
Максимальная высота на которую поднимется тело, брошенное вертикально вверх с начальной скоростью v0, время подъема этого тела на максимальную высоту, и полное время полета (до возвращения в исходную точку):

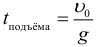

Формула для тормозного пути тела:

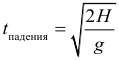
Время падения тела при горизонтальном броске с высоты H может быть найдено по формуле:
Дальность полета тела при горизонтальном броске с высоты H:
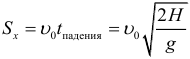
Полная скорость в произвольный момент времени при горизонтальном броске, и угол наклона скорости к горизонту:


Максимальная высота подъема при броске под углом к горизонту (относительно начального уровня):
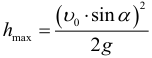
Время подъема до максимальной высоты при броске под углом к горизонту:
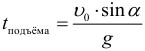
Дальность полета и полное время полета тела брошенного под углом к горизонту (при условии, что полет заканчивается на той же высоте с которой начался, т.е. тело бросали, например, с земли на землю):
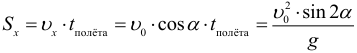

Определение периода вращения при равномерном движении по окружности:

Определение частоты вращения при равномерном движении по окружности:
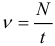
Связь периода и частоты:

Линейная скорость при равномерном движении по окружности может быть найдена по формулам:
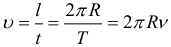
Угловая скорость вращения при равномерном движении по окружности:

Связь линейной и скорости и угловой скорости выражается формулой:

Связь угла поворота и пути при равномерном движении по окружности радиусом R (фактически, это просто формула для длины дуги из геометрии):

Центростремительное ускорение находится по одной из формул:

Равномерное движение по окружности
В качестве дополнения, в таблице ниже приводим всевозможные взаимосвязи между характеристиками тела равномерно вращающегося по окружности (T – период, N – количество оборотов, v – частота, R – радиус окружности, ω – угловая скорость, φ – угол поворота (в радианах), υ – линейная скорость тела, an – центростремительное ускорение, L – длина дуги окружности, t – время):

Химическое количество вещества находится по одной из формул:
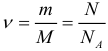
Масса одной молекулы вещества может быть найдена по следующей формуле:

Связь массы, плотности и объёма:

Основное уравнение молекулярно-кинетической теории (МКТ) идеального газа:
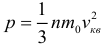
Определение концентрации задаётся следующей формулой:

Для средней квадратичной скорости молекул имеется две формулы:
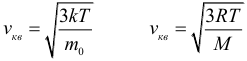
Средняя кинетическая энергия поступательного движения одной молекулы:
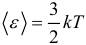
Постоянная Больцмана, постоянная Авогадро и универсальная газовая постоянная связаны следующим образом:
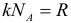
Следствия из основного уравнения МКТ:

Уравнение состояния идеального газа (уравнение Клапейрона-Менделеева):
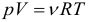
Газовые законы. Закон Бойля-Мариотта:


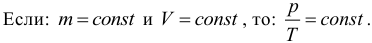
Универсальный газовый закон (Клапейрона):

Давление смеси газов (закон Дальтона):
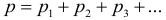
Тепловое расширение тел. Тепловое расширение газов описывается законом Гей-Люссака. Тепловое расширение жидкостей подчиняется следующему закону:

Для расширения твердых тел применяются три формулы, описывающие изменение линейных размеров, площади и объема тела:
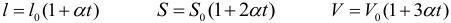
Импульс
Импульс тела находится по следующей формуле:
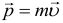
Изменение импульса тела или системы тел (обратите внимание, что разность конечного и начального импульсов векторная):
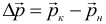
Общий импульс системы тел (важно то, что сумма векторная):

Второй закон Ньютона в импульсной форме может быть записан в виде следующей формулы:
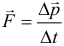
Закон сохранения импульса. Как следует из предыдущей формулы, в случае если на систему тел не действует внешних сил, либо действие внешних сил скомпенсировано (равнодействующая сила равна нолю), то изменение импульса равно нолю, что означает, что общий импульс системы сохраняется:

Если внешние силы не действуют только вдоль одной из осей, то сохраняется проекция импульса на данную ось, например:

Электрический ток
Сила тока может быть найдена с помощью формулы:


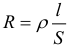
Зависимость сопротивления проводника от температуры задаётся следующей формулой:

Закон Ома (выражает зависимость силы тока от электрического напряжения и сопротивления):
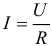
Закономерности последовательного соединения:

Закономерности параллельного соединения:

Электродвижущая сила источника тока (ЭДС) определяется с помощью следующей формулы:

Закон Ома для полной цепи:

Падение напряжения во внешней цепи при этом равно (его еще называют напряжением на клеммах источника):

Сила тока короткого замыкания:
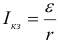
Работа электрического тока (закон Джоуля-Ленца). Работа А электрического тока протекающего по проводнику обладающему сопротивлением преобразуется в теплоту Q выделяющуюся на проводнике:

Мощность электрического тока:
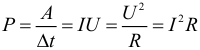
Энергобаланс замкнутой цепи
Полезная мощность или мощность, выделяемая во внешней цепи:

Максимально возможная полезная мощность источника достигается, если R = r и равна:
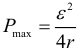
Если при подключении к одному и тому же источнику тока разных сопротивлений R1 и R2 на них выделяются равные мощности то внутреннее сопротивление этого источника тока может быть найдено по формуле:
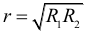
Мощность потерь или мощность внутри источника тока:
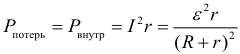
Полная мощность, развиваемая источником тока:

КПД источника тока:

Электролиз
Масса m вещества, выделившегося на электроде, прямо пропорциональна заряду Q, прошедшему через электролит:
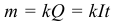
Величину k называют электрохимическим эквивалентом. Он может быть рассчитан по формуле:

Где: n – валентность вещества, NA – постоянная Авогадро, M – молярная масса вещества, е – элементарный заряд. Иногда также вводят следующее обозначение для постоянной Фарадея:

Второй закон Ньютона:
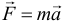
Здесь: F – равнодействующая сила, которая равна сумме всех сил действующих на тело:
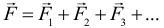
Второй закон Ньютона в проекциях на оси (именно такая форма записи чаще всего и применяется на практике):
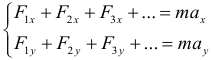
Третий закон Ньютона (сила действия равна силе противодействия):

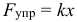
Общий коэффициент жесткости параллельно соединённых пружин:

Общий коэффициент жесткости последовательно соединённых пружин:

Сила трения скольжения (или максимальное значение силы трения покоя):

Закон всемирного тяготения:

Если рассмотреть тело на поверхности планеты и ввести следующее обозначение:

Где: g – ускорение свободного падения на поверхности данной планеты, то получим следующую формулу для силы тяжести:
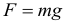
Ускорение свободного падения на некоторой высоте от поверхности планеты выражается формулой:
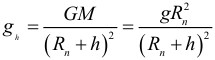
Скорость спутника на круговой орбите:
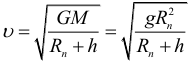
Первая космическая скорость:
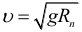
Закон Кеплера для периодов обращения двух тел вращающихся вокруг одного притягивающего центра:
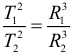
Статика
Момент силы определяется с помощью следующей формулы:

Условие при котором тело не будет вращаться:
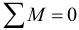
Координата центра тяжести системы тел (аналогичные уравнения для остальных осей):
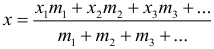
Магнетизм
Сила Ампера, действующая на проводник с током помещённый в однородное магнитное поле, рассчитывается по формуле:
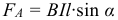
Момент сил действующих на рамку с током:

Сила Лоренца, действующая на заряженную частицу движущуюся в однородном магнитном поле, рассчитывается по формуле:
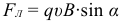
Радиус траектории полета заряженной частицы в магнитном поле:
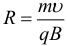
Модуль индукции B магнитного поля прямолинейного проводника с током I на расстоянии R от него выражается соотношением:

Индукция поля в центре витка с током радиусом R:

Внутри соленоида длиной l и с количеством витков N создается однородное магнитное поле с индукцией:
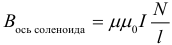
Магнитная проницаемость вещества выражается следующим образом:

Магнитным потоком Φ через площадь S контура называют величину заданную формулой:
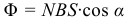
ЭДС индукции рассчитывается по формуле:
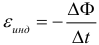
При движении проводника длиной l в магнитном поле B со скоростью v также возникает ЭДС индукции (проводник движется в направлении перпендикулярном самому себе):
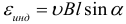
Максимальное значение ЭДС индукции в контуре состоящем из N витков, площадью S, вращающемся с угловой скоростью ω в магнитном поле с индукцией В:


Где: n – концентрация витков на единицу длины катушки:
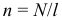
Связь индуктивности катушки, силы тока протекающего через неё и собственного магнитного потока пронизывающего её, задаётся формулой:
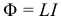
ЭДС самоиндукции возникающая в катушке:
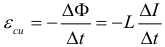
Энергия катушки (вообще говоря, это энергия магнитного поля внутри катушки):

Объемная плотность энергии магнитного поля:

Количество теплоты (энергии) необходимое для нагревания некоторого тела (или количество теплоты выделяющееся при остывании тела) рассчитывается по формуле:
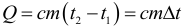
Теплоемкость (С – большое) тела может быть рассчитана через удельную теплоёмкость (c – маленькое) вещества и массу тела по следующей формуле:
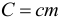
Тогда формула для количества теплоты необходимой для нагревания тела, либо выделившейся при остывании тела может быть переписана следующим образом:

Фазовые превращения. При парообразовании поглощается, а при конденсации выделяется количество теплоты равное:

При плавлении поглощается, а при кристаллизации выделяется количество теплоты равное:
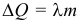
При сгорании топлива выделяется количество теплоты равное:
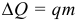
Уравнение теплового баланса (ЗСЭ). Для замкнутой системы тел выполняется следующее (сумма отданных теплот равна сумме полученных):
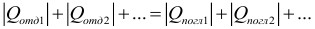
Если все теплоты записывать с учетом знака, где «+» соответствует получению энергии телом, а «–» выделению, то данное уравнение можно записать в виде:

Работа идеального газа:
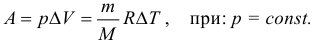
Если же давление газа меняется, то работу газа считают, как площадь фигуры под графиком в p–V координатах. Внутренняя энергия идеального одноатомного газа:

Изменение внутренней энергии рассчитывается по формуле:

Первый закон (первое начало) термодинамики (ЗСЭ):
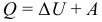
Для различных изопроцессов можно выписать формулы по которым могут быть рассчитаны полученная теплота Q, изменение внутренней энергии ΔU и работа газа A. Изохорный процесс (V = const):

Изобарный процесс (p = const):

Изотермический процесс (T = const):
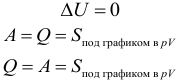
Адиабатный процесс (Q = 0):

КПД тепловой машины может быть рассчитан по формуле:
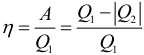
Где: Q1 – количество теплоты полученное рабочим телом за один цикл от нагревателя, Q2 – количество теплоты переданное рабочим телом за один цикл холодильнику. Работа совершенная тепловой машиной за один цикл:

Наибольший КПД при заданных температурах нагревателя T1 и холодильника T2, достигается если тепловая машина работает по циклу Карно. Этот КПД цикла Карно равен:
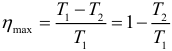
Абсолютная влажность рассчитывается как плотность водяных паров (из уравнения Клапейрона-Менделеева выражается отношение массы к объему и получается следующая формула):

Относительная влажность воздуха может быть рассчитана по следующим формулам:


Потенциальная энергия поверхности жидкости площадью S:

Сила поверхностного натяжения, действующая на участок границы жидкости длиной L:
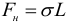
Высота столба жидкости в капилляре:

При полном смачивании θ = 0°, cos θ = 1. В этом случае высота столба жидкости в капилляре станет равной:
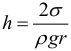
При полном несмачивании θ = 180°, cos θ = –1 и, следовательно, h < 0. Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
Гидростатика
Определение давления задаётся следующей формулой:
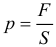
Давление, которое создает столб жидкости находится по формуле:

Но часто нужно учитывать еще и атмосферное давление, тогда формула для общего давления на некоторой глубине h в жидкости приобретает вид:
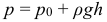
Идеальный гидравлический пресс:
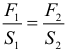

Любой гидравлический пресс:
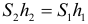
КПД для неидеального гидравлического пресса:
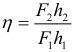
Сила Архимеда (выталкивающая сила, V – объем погруженной части тела):
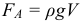
Электростатика
Электрический заряд может быть найден по формуле:

Линейная плотность заряда:

Поверхностная плотность заряда:
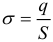
Объёмная плотность заряда:
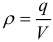
Закон Кулона (сила электростатического взаимодействия двух электрических зарядов):
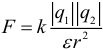
Где: k – некоторый постоянный электростатический коэффициент, который определяется следующим образом:
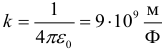
Напряжённость электрического поля находится по формуле (хотя чаще эту формулу используют для нахождения силы действующей на заряд в данном электрическом поле):
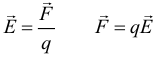
Принцип суперпозиции для электрических полей (результирующее электрическое поле равно векторной сумме электрических полей составляющих его):

Напряженность электрического поля, которую создает заряд Q на расстоянии r от своего центра:

Напряженность электрического поля, которую создает заряженная плоскость:

Потенциальная энергия взаимодействия двух электрических зарядов выражается формулой:

Электрическое напряжение это просто разность потенциалов, т.е. определение электрического напряжения может быть задано формулой:

В однородном электрическом поле существует связь между напряженностью поля и напряжением:

Работа электрического поля может быть вычислена как разность начальной и конечной потенциальной энергии системы зарядов:

Работа электрического поля в общем случае может быть вычислена также и по одной из формул:
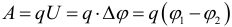
В однородном поле при перемещении заряда вдоль его силовых линий работа поля может быть также рассчитана по следующей формуле:

Определение потенциала задаётся выражением:
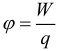
Потенциал, который создает точечный заряд или заряженная сфера:
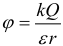
Принцип суперпозиции для электрического потенциала (результирующий потенциал равен скалярной сумме потенциалов полей составляющих итоговое поле):

Для диэлектрической проницаемости вещества верно следующее:
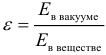
Определение электрической ёмкости задаётся формулой:
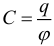
Ёмкость плоского конденсатора:


Напряжённость электрического поля внутри плоского конденсатора:

Сила притяжения пластин плоского конденсатора:

Энергия конденсатора (вообще говоря, это энергия электрического поля внутри конденсатора):
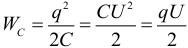
Объёмная плотность энергии электрического поля:
Расширенная PDF версия документа “Все главные формулы по школьной физике”
Пример
1.
Определить число атомов N,
содержащихся в 1 кг гелия. Найти массу
m0
одного атома гелия.
Решение:
Поскольку
гелий – одноатомный газ, то число атомов
в данной массе газа
где
= m
/М –
количество молей вещества, М
– молярная масса, m
– масса газа, NА
– число Авогадро.
Найдём
искомое число атомов

Для
определения массы m0
одного атома массу m
газа разделим на число атомов N
в нём:

Ответ:
N
= 1,5·1026;
m
= 6,67·10–26
кг.
Пример
2.
Считая водород в солнечной фотосфере
(внешней видимой оболочке Солнца)
идеальным газом, определить среднюю
кинетическую энергию

Решение:
Связь между давлением р
идеального газа, концентрацией n
и средней кинетической энергиейтеплового
движения частиц



Пример
3.
Найти наиболее вероятную υв,
среднюю арифметическую

и среднюю квадратичную

скорости молекул водорода при температуре
27 С.
Решение:
В
газе, находящемся в состоянии равновесия,
устанавливается некоторое стационарное,
не меняющееся со временем распределение
молекул по скоростям, которое подчиняется
статистическому распределению Максвелла.
Распределение
Максвелла (рис. 1) позволяет определить
относительное число молекул ∆N(υ)/N,
скорости которых лежат в интервале от
υ
до υ+∆υ.
Скорость
υв,
которой соответствует максимум кривой
распределения Максвелла, называют
наиболее
вероятной скоростью.
Этой скоростью и близкой к ней при данной
температуре обладает наибольшее число
молекул.
Наиболее
вероятную скорость найдем по формуле
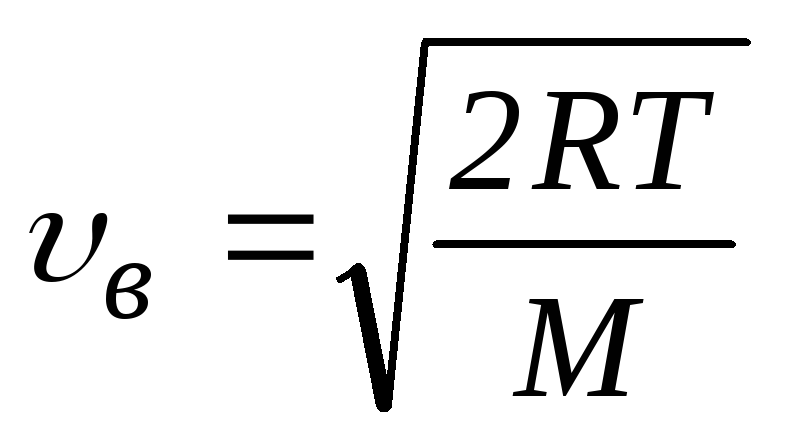
,
(1)
где
R
– молярная газовая постоянная, Т
– абсолютная температура,
М
– масса одного моля газа.


по
определению равна отношению суммы
скоростей всех молекул к числу молекул:
Из
закона распределения Максвелла средняя
арифметическая скорость молекул
определяется следующим образом:



определяет среднюю кинетическую энергию
движения молекулы. Средняя кинетическая
энергия поступательного движения


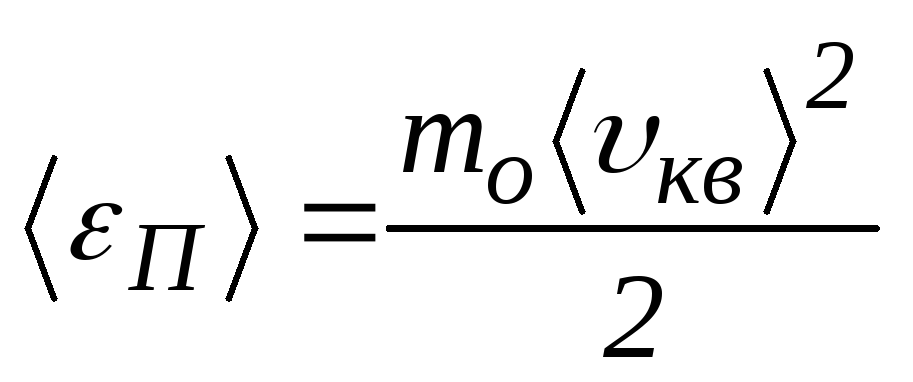
Сравнивая
(5) и (6), находим


Ответ:
υв
= 1,58 км/с;

Пример
4.
Считая водяной пар массой m=
180 г при температуре
t
= 127 oС
идеальным газом, определить: энергию,
приходящуюся на одну степень свободы
молекулы

;
среднюю кинетическую энергию
поступательного

и среднюю кинетическую энергию
вращательного движения
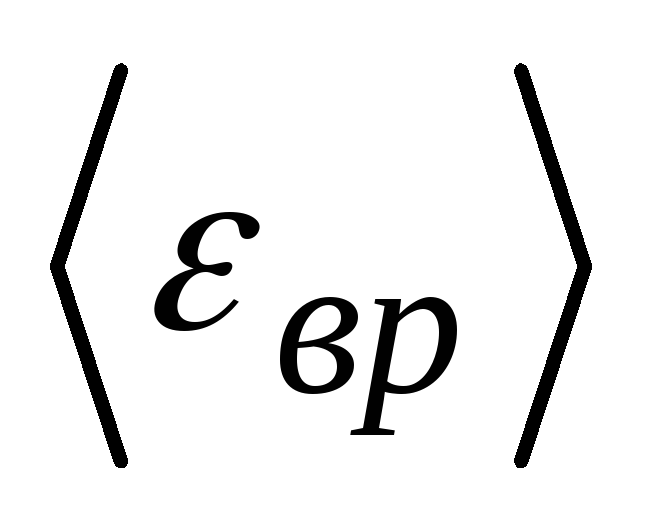
одной молекулы водяного пара, а также
кинетическую энергию W
всех молекул водяного пара и его
внутреннюю энергию U
.
Решение:
По закону Больцмана энергия равномерно
распределяется по степеням свободы. На
одну степень свободы приходится энергия
где
k
– постоянная Больцмана.
Для
идеальных одноатомных газов (атомарного
кислорода, атомарного азота, атомарного
водорода, гелия) учитываются только три
степени поступательного движения (i
= 3). Для двухатомных газов (например,
молекулярного кислорода, молекулярного
водорода) учитываются три степени
поступательного движения и две степени
вращательного движения (i
= 5).
Для газов, молекулы которых состоят из
трёх и более атомов, учитываются три
степени поступательного движения и три
степени вращательного движения молекул
(i
= 6).
Так
как молекула водяного пара является
трёхатомной, то обладает тремя степенями
свободы поступательного движения и
тремя степенями свободы вращательного
движения.
Следовательно,
средняя энергия поступательного движения
одной молекулы водяного пара

.
(2)
Средняя
кинетическая энергия вращательного
движения одной молекулы водяного пара

.
(3)
Полная
энергия одной молекулы водяного пара
равна сумме энергий поступательного и
вращательного движения:

.
(4)
Полная
кинетическая энергия всех N
молекул водяного пара выражается
соотношением:
Если
учесть, что число молекул N
системы равно произведению постоянной
Авогадро NA
на количество вещества ν,
то равенство (5) можно записать в виде:
По
определению, внутренняя энергия
идеального газа равна полной кинетической
энергии всех его молекул, то есть U
= 99,7 Дж.
Пример
5.
Определить плотность смеси газов,
состоящей из
5 моль азота и 10 моль
кислорода. Смесь содержится в баллоне
при температуре t
= 17 oС
и давлении Рсм
= 0,25 МПа.
Решение:
Согласно определению плотность газовой
смеси
где
m1
и m2
–
массы азота
и кислорода соответственно,
V
–
объём баллона.
Выразим
массу каждого газа через количество
вещества
и молярную массу M
m1
= ν1M1,
m2
= ν2M2.
(2)
Для
определения объёма смеси в баллоне
воспользуемся уравнением Клапейрона–Менделеева
где
R
–
молярная газовая постоянная; Т
–
термодинамическая температура.
Объём смеси в
баллоне
Подставив выражения
(2) и (3) в (1), получим

.
(4)
Ответ:
= 3,18 кг/м3.
Пример
6.
Определить среднюю длину свободного
пробега

и среднюю частоту столкновений

молекул
воздуха при температуре
t
= 0 °С и давлении р
= 1,01 Па. Принять эффективный диаметр
молекулы воздуха равнымd
= 2,9·10-8
см.
Решение:
Средняя
длина свободного пробега молекулы
выражается формулой

,
(1)
где
п
–
концентрация молекул (отношение числа
молекул к объёму газа, в котором они
заключены).
Найдем
неизвестную концентрацию молекул,
используя основное уравнение
молекулярно-кинетической теории и
определение средней энергии поступательного
движения молекулы газа

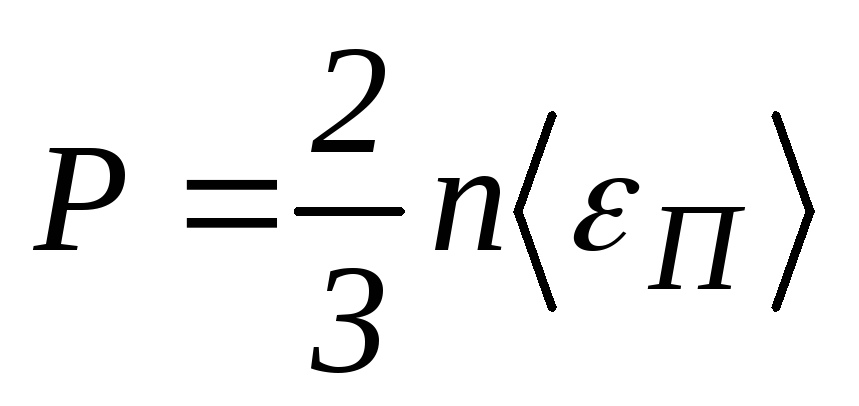

,
(3)
где
р
–
давление газа, k
–
постоянная Больцмана, Т
–
термодинамическая температура газа.
С учётом уравнений
(2) и (3) формула (1) примет вид
Отсюда
искомая длина свободного пробега
молекулы

молекул
газа связана с длиной
свободного пробега



– средняя
арифметическая скорость молекул.
Её
можно определить по формуле
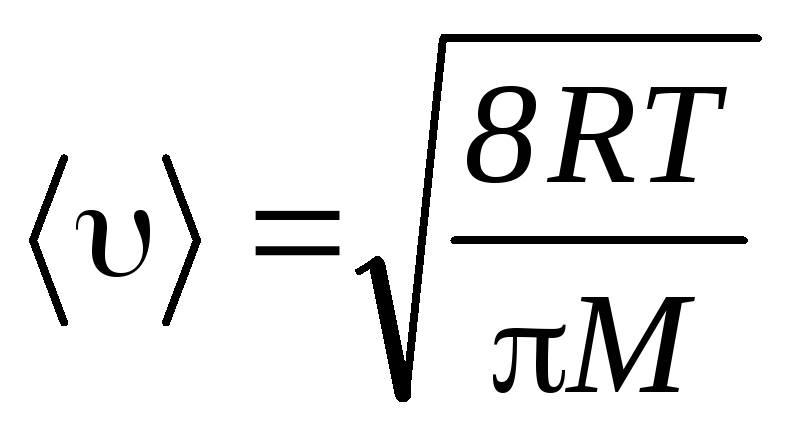
,
(6)
где
R
–
молярная газовая постоянная, М
– молярная масса воздуха.
Подставив (6) в (5),
находим

= 1 см;

Пример
7. Найти,
при каком градиенте плотности углекислого
газа через каждый квадратный метр
поверхности почвы продиффундирует в
атмосферу в течение t
= 1 ч газ массой
m
= 720 мг, если коэффициент диффузии D
= 0,04 см2/с.
Решение:
Масса газа, переносимая в результате
диффузии, определяется законом Фика:

,
(1)
где
D
–
коэффициент диффузии; ∆ρ/∆x
–
градиент плотности, т.е. изменение
плотности, приходящееся на 1 м толщины
слоя почвы;
S
– площадь поверхности слоя; t
– длительность процесса.
Из (1) выразим
искомый градиент плотности
Отрицательное
значение градиента плотности соответствует
сущности процесса диффузии: зависимость
плотности от расстояния в направлении
движения диффундирующей массы выражается
убывающей функцией, градиент которой
– отрицательная величина.
Ответ:
∆ρ/∆x
= –0,05 кг/м4.
Пример
8.
Определить
количество теплоты, теряемое через
бетонные стены склада площадью S
= 50 м2
за время t
= 1 мин, если в помещении температура
стены t1
= 15 °C,
а снаружи t2
=
–10 °С. Толщина стен ∆x
= 25 см.
Решение:
Количество теплоты, передаваемое за
счёт теплопроводности стен, выражается
законом Фурье:

,
(1)
где
λ
– теплопроводность материала стены;
∆T/∆x
–
градиент температуры, т.е. изменение
температуры, приходящееся на 1м толщины
стены; S
– площадь
поверхности стены; t
– время процесса.
Подставим
числовые значения величин в формулу
(1) и вычислим теряемое количество
теплоты:
Ответ:
Q
= 245 кДж.
Пример
9. При
изобарном нагревании некоторого газа
массой
m
= 0,5 кг на ∆Т
= 10 К требуется на 1,48 кДж количества
теплоты больше, чем при изохорном
нагревании. Определить для этого газа
удельные теплоёмкости при постоянном
давлении
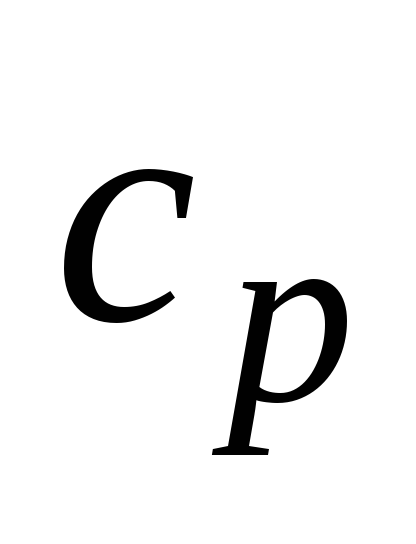
и
при постоянном объёме

.
Какой это газ?
Решение:
В
соответствии с первым началом термодинамики
при изобарном нагревании газ получает
количество теплоты QР:
QР
=∆U
+ A,
(1)
где
∆U
– изменение внутренней энергии газа,
А
–
работа, совершённая газом.
При изобарном
расширении
А
= р ∆V,
(2)
где
р
– давление газа, ∆V
– изменение объёма газа.


,
(3)
где
R
–
молярная газовая постоянная.
При
изохорном нагревании газ работу не
совершает и полученное им количество
теплоты QV
расходуется только на увеличение
внутренней энергии газа ∆U,
поэтому
С
учётом выражений (2), (3) и (4) уравнение
(1) примет вид

.
(5)
По
условию задачи ∆Q
= QР
– QV
,
следовательно
Выразим
молярную массу газа М:
Данную
молекулярную массу имеет молекулярный
азот N2
(двухатомный газ, у которого число
степеней свободы i
= 5).
Пример
10.
Кислород занимает объём V1
= 1 м3
и находится под давлением р1
= 200 кПа. Его нагрели сначала при постоянном
давлении до объёма V2
= 3 м3,
а затем при постоянном объёме до
давления
р2
= 500 кПа. Построить график процесса и
найти: совершённую газом работу А;
изменение ∆U
внутренней энергии и количество теплоты
Q,
переданное газу.
Решение:
На
рис. 2 показан график перехода газа из
состояния 1 в состояние 3 при изобарном,
а затем при изохорном нагревании. На
графике точками 1, 2, 3 обозначены состояния
газа, характеризуемые параметрами (р1,
V1,
Т1),
(р2,
V2,
Т2),
(р3,
V3,
Т3).
Изменение
внутренней энергии газа при переходе
его из состояния 1 в состояние 3 выражается
формулой
где
i
– число степеней свободы газа (для
кислорода, молекулы которого состоят
из двух атомов, i
= 5); m
– масса газа; М
– молярная масса газа;
R
– молярная газовая постоянная.
Температуры
Т1
и Т3
можно найти из уравнения Клапейрона–Менделеева
(

Следовательно,
равенство (1) примет вид:

.
(3)
Полная
работа, совершаемая газом,
А
= А12
+ А23, (4)
где
А12
– работа газа при изобарном нагревании
из состояния 1 в состояние 2; А23
– работа газа при изохорном переходе
газа из состояния 2 в состояние 3.
При
любом процессе работа может быть найдена
графически, как площадь под кривой
конкретного процесса в координатах Р,
V.
При переходе 1-2 работа А12
равна
площади прямоугольника (заштрихованная
часть графика на рис. 2):
А
= р1∆V
= p1(V2–
V1).
(5)
В
изохорном процессе объем газа не
изменяется, поэтому работа
А23
= 0. Таким образом,
А
= А12=
p1(V2
–
V1).
(6)
В
результате вычислений получим:
А
= 2∙105∙(3–1)
Дж = 4∙105
Дж = 0,4 МДж.
Согласно
первому началу термодинамики, количество
теплоты Q,
переданное газу, расходуется на изменение
внутренней
энергии ∆U
и на совершение газом работы
А:
Q
= ∆
U
+ А. (7)
Подставляя
в (7) значения величин, получим Q
= 3,65 МДж.
Ответ:
А
= 0,4 МДж;
∆U
=
3,25 МДж;
Q
= 3,65 МДж.
Пример
11.
Воздух,
взятый при температуре t1
= 0 °C, был адиабатно сжат так, что его
объём уменьшился в три раза. Определить
температуру t2
воздуха
после сжатия.
Решение:
Зависимость между температурой и объёмом
при адиабатном сжатии выражается
уравнением Пуассона:
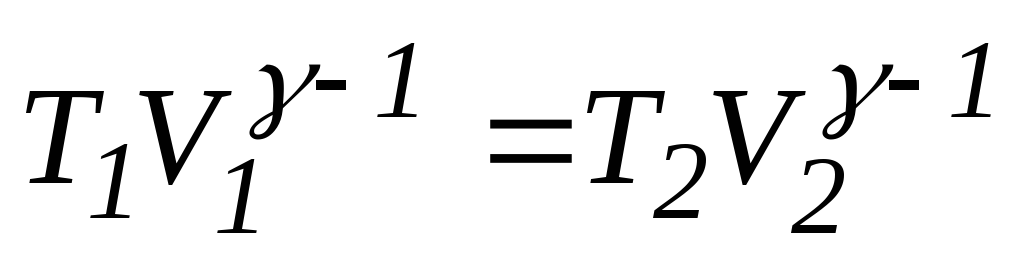
,
(1)
где
T1,V1
– термодинамическая температура и
объём до сжатия воздуха; T2,
V2
– те же величины после сжатия воздуха;
– коэффициент Пуассона.
где
сP
и
сV
– удельные теплоёмкости газа при
постоянном давлении и объёме соответственно.
Из
теории теплоёмкостей газов известно,
что
Подставив
(3) и (4) в (2), получим
где
i
– число степеней свободы молекулы газа.
Сухой
воздух состоит в основном из молекулярных
кислорода (О2)
и азота (N2),
для которых i
= 5.
Следовательно,
=
(5 + 2)/5 = l,4.
Из формулы (1)
получим
Вычислим
температуру конечного состояния:
Т2
=
273∙31,4–1
К = 273∙30,4
К.
Прологарифмируем
обе части равенства (5):
lnT2
= ln273
+ 0,4∙ln3
= 5,61 + 0,4∙1,1 = 10,01.
Отсюда
T2
= 424 К или t2
= (Т2
– 273) С
= 151 С.
Пример
12.
Кислород массой m
= 0,45 г имеет в начальном состоянии объём
V1
= 2 л и температуру t1
= 10 C,
а в конечном – объём
V2
= 10 л и температуру t2
= 50 C.
Найти изменение энтропии ∆S
кислорода
при переходе из первого состояния во
второе.
Решение:
Изменение энтропии
(приведённое количество теплоты)
определяется формулой

,
(1)
где
δQ
– элементарное количество теплоты,
сообщённое газу при данной температуре;
Т
– термодинамическая температура.
В
соответствии с первым началом термодинамики
для идеального газа элементарное
количество теплоты
δQ
=dU
+ δA,
(2)
где
dU
–
изменение внутренней энергии газа; δA
– элементарная работа газа.

,
(3)
где
m
– масса газа; М
– молярная масса газа; R
– молярная газовая постоянная; i
– число степеней свободы (кислород –
двухатомный газ,
i
= 5).
Элементарная
работа расширения газа рассчитывается
по формуле
где
p
–
давление газа; dV
– элементарное изменение объёма газа.
Давление
p
можно найти из уравнения Клапейрона–Менделеева:
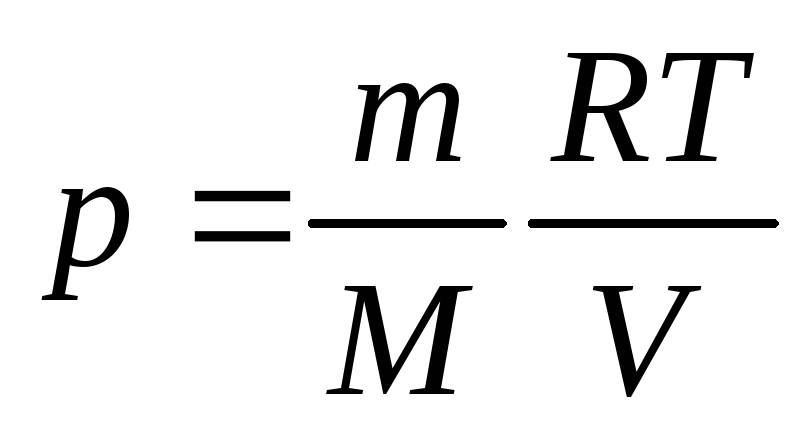
.
(5)
Подставив
(3), (4), (5) в (2), определяем количество
теплоты δQ,
полученное газом при переходе из
состояния 1 в состояние 2:

.
(6)
В
результате интегрирования изменение
энтропии

.
(7)
Пример
13. Идеальный
двухатомный газ, содержащий 1 кмоль
количества вещества, совершает замкнутый
цикл, график которого приведён на рис.
3. Определить работу А,
совершаемую газом за цикл; термический
кпд
цикла
η;
количество теплоты Q2,
переданное холодильнику, если в процессах
1-2 и 2-3 газ получает количество теплоты
Q1
= 7,6 кДж.
Решение:
Цикл
состоит из двух изохор (процессы 1-2, 3-4)
и двух изобар (процессы 2-3, 4-1). Общая
работа за цикл равна сумме работ,
совершаемых в каждом процессе цикла:
А
= А12
+ A23
+ А34
+ А41. (1)
При
изохорных процессах изменение объёма
газа ∆V
=
0, следовательно, работы
А12
= А34
= 0. (2)
При
изобарных процессах 2-3, 4-1 работы А23
и
А41
можно найти по формулам:
A23
= p2
∆V23
= p2(V3
– V2),
(3)
A41
= p1
∆V41
= p1(V1
– V4).
(4)
Числовые
значения давлений и объёмов определяем
из графика:
p1
=
12 кПа;
p2
=
16 кПа; V1
= V2
=
2 м3;
V3
= V4
= 3 м3.
Рассчитаем
работы A23
и
A41:
A23
= 16∙103
(3
– 2) Дж = 16 кДж, A41
= 12∙103
(2
– 3) Дж = –12 кДж.
Таким образом,
работа за цикл
А
=
( А23
–
А41)
= 4 кДж.
На
графике в координатах
р,
V
работа за цикл изображена заштрихованной
площадью.
По
определению термический коэффициент
полезного действия η
где
Q1
– количество теплоты, переданное
нагревателю, Q2
– количество теплоты, переданное
холодильнику.
Подставляя
числовые значения, получим:

Количество
теплоты Q2,
переданное холодильнику, найдём из
формулы (5):
Q2
= (1– η)∙Q1,
(6)
отсюда
Q2
=
(1– 0,53)∙7,6∙103
Дж = 3,6∙103
Дж = 3,6 кДж.
Ответ:
А
=
4 кДж; η
= 53%; Q2
=
3,6 кДж.
Пример
14. На
какую высоту может подняться вода в
капиллярном канале диаметром d
= 0,08 мм в стебле ржи? Смачивание считать
полным.
Решение:
По условию задачи вода полностью
смачивает стебель. Со стороны стебля
на каждый бесконечно малый элемент
длины линии соприкосновения воды со
стеблем действует сила, направленная
вверх (рис. 4). Результирующая всех сил,
действующих на линию соприкосновения,
также направлена вверх и определяется
по формуле
F
= 2πr,
(1)
где
r
– радиус капилляра,
– коэффициент поверхностного натяжения
воды.
Сила
F
вызывает подъём воды в капилляре до тех
пор, пока не будет уравновешена силой
тяжести, действующей на весь поднятый
столб воды. Условием равновесия является
равенство
F
= mg.
(2)
Масса
поднятого столба воды
m
= V
= πr2h, (3)
где
–
плотность воды,
V
– объём поднятого слоя.
С
учётом (1) и (3) формула (2) примет вид:
2πr
= πr2hg.
(4)

.
(5)
Рассчитываем
высоту поднятия воды в стебле ржи:
Ответ:
h
= 36,5 см.
Соседние файлы в папке Физика_Шилова
Оптика
Оптическая длина пути определяется формулой:

Оптическая разность хода двух лучей:
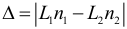
Условие интерференционного максимума:

Условие интерференционного минимума:
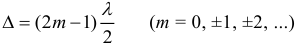
Формула дифракционной решетки:
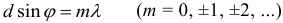
Закон преломления света на границе двух прозрачных сред:

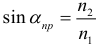
Формула тонкой линзы:
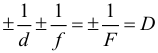
Линейным увеличением линзы Γ называют отношение линейных размеров изображения и предмета:

Атомная и ядерная физика
Энергия кванта электромагнитной волны (в т.ч. света) или, другими словами, энергия фотона вычисляется по формуле:
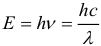

Формула Эйнштейна для внешнего фотоэффекта (ЗСЭ):
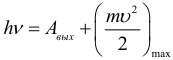
Максимальная кинетическая энергия вылетающих электронов при фотоэффекте может быть выражена через величину задерживающего напряжение Uз и элементарный заряд е:
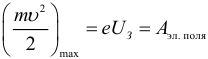
Существует граничная частота или длинна волны света (называемая красной границей фотоэффекта) такая, что свет с меньшей частотой или большей длиной волны не может вызвать фотоэффект. Эти значения связаны с величиной работы выхода следующим соотношением:

Второй постулат Бора или правило частот (ЗСЭ):

В атоме водорода выполняются следующие соотношения, связывающие радиус траектории вращающегося вокруг ядра электрона, его скорость и энергию на первой орбите с аналогичными характеристиками на остальных орбитах:
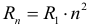
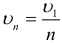
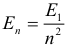
На любой орбите в атоме водорода кинетическая (К) и потенциальная (П) энергии электрона связаны с полной энергией (Е) следующими формулами:
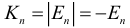

Общее число нуклонов в ядре равно сумме числа протонов и нейтронов:
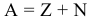
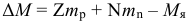
Энергия связи ядра выраженная в единицах СИ:
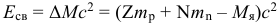
Энергия связи ядра выраженная в МэВ (где масса берется в атомных единицах):
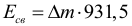
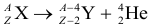
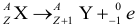
Закон радиоактивного распада:

Ядерные реакции
Для произвольной ядерной реакции описывающейся формулой вида:

Выполняются следующие условия:

Энергетический выход такой ядерной реакции при этом равен:








