Рфэс – основной метод неразрушающего анализа поверхности
Одним из основных направлений современных технологий является использование специфических свойств материалов и применение этих свойств как в существующих, так и в новых проектах с целью их усовершенствования. Поэтому в последние десятки лет очень большое внимание уделяется изучению поверхности материалов.
Рентгеновская фотоэлектронная спектроскопия РФЭС (XPS – англ. X-ray photoelectron spectroscopy) является широко используемым методом химического анализа поверхности. В промышленной лаборатории данный метод может применяться для широкого спектра задач, начиная от идентификации загрязнения на поверхности и заканчивая характеристикой материалов в качестве контроля процесса или в качестве метода определения характеристик новых материалов в исследовательской среде. Для более подробного анализа может потребоваться визуализация образца или профили по глубине, а также использование численных методов, таких как аппроксимация кривой, послойное моделирование или подбор линейных наименьших квадратов для более точного описания материала.
Методы фотоэлектронной спектроскопии
Физической основой методов фотоэлектронной спектроскопии (ФЭС) служит внешний фотоэффект. Фотон с энергией hv поглощается электроном с энергией связи Eg ниже уровня вакуума. Если энергии фотона достаточно для разрыва связи и преодоления электроном поверхностного потенциального барьера, он покидает твердое тело с кинетической энергией EKllH=hv -Ед-щ, где Фо = ^вакуум–
—?ферМи – работа выхода материала. Электроны, покинувшие твердое
тело в результате внешнего фотоэффекта, называются фотоэлектронами.
Энергию, достаточную для преодоления поверхностного потенциального барьера, могут сохранить только те электроны, которые эмитировали с глубины, не превышающей несколько их нанометров. В простейшем случае энергетическое распределение фотоэлектронов совпадает с распределением электронных состояний на поверхности твердого тела, смещенным вверх на величину hv.
Энергия фотонов известна, кинетическая энергия фотоэлектрона Екин регистрируется с помощью спектрометра, а работа выхода легко определяется с помощью калибровочных экспериментов. Значит, легко можно найти энергию связи (ионизации) соответствующего электронного уровня, которая зависит от характера распределения электронов в исследуемой системе (рис. 3.36).
Но на самом деле, поскольку вероятность поглощения фотона для различных электронных состояний различна, все оказывается несколько сложнее.
Для регистрации фотоэлектронов должны быть выполнены следующие условия [5]:
- • энергия фотона должна быть достаточна, чтобы электрон смог покинуть твердое тело, т. е. hv > Eg –Тфо ;
- • электрон не должен потерять энергию в столкновениях с другими электронами на своем пути к поверхности;
- • скорость электрона должна быть направлена в сторону внешней поверхности.
![Процесс фотоэмиссии электронов [17]](https://studref.com/htm/img/39/8502/221.png)
Рис. 3.36.Процесс фотоэмиссии электронов [17]

Рис. 3.37.Схематическое изображение процессов:
а – ультрафиолетовой фотоэлектронной спектроскопии; б – рентгеновской фотоэлектронной спектроскопии [7]
Все методы ФЭС заключаются в получении спектров энергетического распределения фотоэлектронов, эмитируемых твердым телом при облучении потоком монохроматического электромагнитного излучения. В зависимости от спектрального диапазона излучения, падающего на образец, различают две разновидности ФЭС:
1) рентгеновскую фотоэлектронную спектроскопию (РФЭС) (XRS – X-Ray Spectroscopy или XPS), в которой используется рентгеновское излучение с энергией квантов в диапазоне от 100 эВ до 10 кэВ (соответствующие длины волн в диапазоне от 100 до 1 А);
2) ультрафиолетовую фотоэлектронную спектроскопию (УФЭС) (UPS – Ultra-violet Photoemission Spectroscopy), в которой используются фотоны ультрафиолетового спектрального диапазона 10…50 эВ (соответствующие длины волн от 1000 до 250 А).
При облучении образца рентгеновским излучением зондируются глубокие остовные уровни (рис. 3.37, б), а при облучении фотонами ультрафиолетового спектрального диапазона возбуждаются электроны валентной зоны (рис. 3.37, а). Деление достаточно условно, так как в обоих методах используются одни и те же физические процессы.
Рентгеновские фотоэлектронные спектрометры для рфэс
В настоящее время нет единого универсального метода, который позволил бы решать все задачи, связанные с поверхностью. Принято полагать, что для полного понимания проблемы поверхности следует использовать набор взаимно дополняющих методов.
В целом, можно предположить, что будут строиться высоковакуумные комплексы, сочетающие в себе методы осаждения твердотельных материалов и исследование новых материалов спектральными, дифракционными и другими методами микроскопии.
PHI VersaProbe III сочетает в себе несколько методов, чтобы получить комплексную информацию о структуре, составе и химическом состоянии поверхности. Автоматизация и высокая производительность системы позволяют проводить анализ образцов в условиях, отвечающих современным требованиям.
Рисунок 6 – Источники, используемые в PHI VersaProbe III
Рисунок 7 – Рабочее место PHI VersaProbe III
Степень окисления
Рентгеноэлектронные спектры позволяют четко показать, что энергия связи внутреннего уровня атома в сильной степени зависит от степени окисления элемента, спектр которого изучается. Так, уже в первых работах было установлено, что при одинаковых ближайших соседях сдвиг внутренних уровней исследуемого атома в сторону увеличения Есв тем больше, чем больше степень окисления элемента в соединении.
При изучении поверхности металлов и сплавов часто возникают вопросы, является ли поверхность окисленной и какой именно компонент сплава окислен. Рентгеноэлектронные спектры в большинстве случаев помогают решить эту задачу, поскольку энергия связи электрона в металле обычно на несколько электронвольт меньше, чем в оксиде, причем с увеличением степени окисления также растет положительный химический сдвиг.
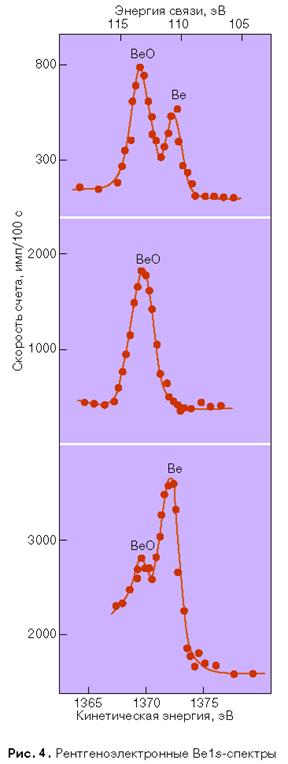 – 4
– 4
торр и осаждался на алюминиевую подложку. Образец облучали рентгеновскими квантами Kα
-линии Al и изучали выбитые 1s-электроны с целью определения энергии связи 1s-электрона в бериллии. Спектр (рис. 4) состоит из двух линий одинаковой интенсивности, расстояние между которыми равно 2,9 ± 0,1 эВ. Появление двух линий вместо одной можно объяснить тем, что металл частично окислен и одна из линий электронного спектра соответствует металлическому, а другая – окисленному бериллию. Для проверки этого предположения образец нагревали на воздухе до полного окисления бериллия и снова снимался электронный спектр. На этот раз была получена только одна 1s-линия. Ее положение совпадает с положением линии меньшей кинетической энергии на рис. 4. Следовательно, это линия бериллия в окисле. Для дополнительного доказательства бериллиевый образец, полученный испарением в вакууме, частично восстанавливали цирконием, после чего был получен его электронный спектр. Хотя в спектре видны обе линии, линия, соответствующая окислу, гораздо менее интенсивна.
Структура молекул
В настоящее время проведены многочисленные исследования, показывающие эффективность применения рентгеноэлектронной спектроскопии для решения различных вопросов структурной химии органических и неорганических соединений. Применение РФЭС в структурной химии можно показать на примере исследования 1s-спектров азота (N1s)
Рентгеноэлектронный спектр Na2
N2
O3
ясно указывает наличие структурно неэквивалентных атомов азота, и это исключает симметричную структуру (I). В то же время можно также ожидать, что структуры II и III будут давать две полосы в спектре N1s.
Типичный анализ по методу рфэс
Типичный анализ РФЭС (например, на рентгеновском спектрометре VersaProbe III от PHI) начинается с получения изображения, которое быстро генерируется с использованием растрового рентгеновского луча диаметром менее 10 мкм. Благодаря полученным изображениям можно определить области, представляющие интерес для спектрального анализа.
Рисунок 2 – Изображение структуры устройства, полученное при сканировании рентгеновским пучком (слева); спектры трех выбранных точек на изображении (справа)
Рисунок 3 – Элементный состав выбранной области (слева); спектры, полученные из областей на элементной карте кремния (справа)
Рисунок 4 – Карта химического состава в выбранной области устройства
Факультет: рэф
Группа: РФ1-32
Студент: Косенков В.Е.
Преподаватель: Величко А.А.
Химический сдвиг
|
 св
св
электронов остова несколько меняется при изменении характера химического окружения атома, спектр которого изучается.
|
Изменения энергии связи (ΔЕ
св
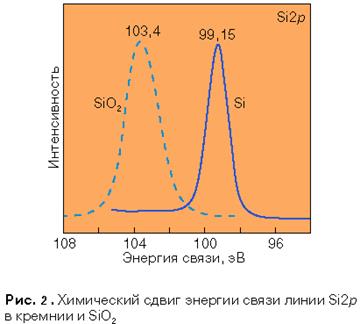
) для электронного уровня одного и того же элемента в разных соединениях принято называть химическим сдвигом. Одними из важнейших результатов, полученных группой шведских физиков, являются демонстрация возможности измерения химических сдвигов на примерах рентгеноэлектронных спектров многих органических и неорганических соединений и создание аппаратуры, способной регистрировать соответствующие сдвиги. Сдвиг энергии внутренних электронов в зависимости от химического окружения показан на рис. 2 для линии Si2p. Энергия связи Si2p смещается более чем на 4 эВ при переходе от Si к SiO
2
. Сдвиг энергии уровня обычно измеряется относительно свободного элемента. Средняя точность экспериментальных значений Е
св
~ ± (0,1-0,2) эВ для твердых тел и около (± 0,04) эВ для газов.
Для иллюстрации зависимости энергии связи электрона в атоме от химического окружения атома часто используют рентгеноэлектронный 1s-спектр углерода этилового эфира трифторуксусной кислоты (рис. 3). Четыре максимума C1s почти равной интенсивности в весьма изящной форме представляют четыре окружения атомов углерода в этой молекуле.
В табл. 2 приведены значения энергий связи для 2p-уровня серы в газообразных соединениях. Из табл. 2 видно, что изменения энергии связи внутренних электронов могут достигать очень значительных величин в ряду соединений этого элемента. 






